將藥物經過皮膚輸送進入人體發揮治療作用,目前主要的制劑形式包括貼劑(如,芬太尼貼)和各種半固體制劑。貼劑在設計時希望較多的藥物穿透皮膚進入系統循環發揮藥效,相比于口服等傳統給途徑,能夠避免首過效應、減輕血藥濃度峰谷波動、減少服藥頻次;半固體的皮膚外用制劑一般更傾向于使藥物透過皮膚表層后停留在皮膚內發揮局部治療作用,具有較少的系統暴露量,降低副作用風險。無論是哪一種治療目的,在研發階段藥物的成藥性評估、制劑處方優化、仿制藥的等效性等研究時,都要進行體外透皮試驗(in vitro permeation test,IVPT)。顯而易見,皮膚與消化道的生理解剖結構差異大,存在阻礙藥物吸收的角質層,因此對于此類制劑非臨床ADME評價的策略及關注點,都有別于其他傳統給藥途徑的制劑。
目前,IVPT廣泛使用Franz擴散池來進行。Franz擴散池包括一個裝有受試藥物的供給室和一個裝有接收液的接收室組成,在使用時兩室之間夾載皮膚或膜材,接收室外部用水浴或金屬加熱套保溫,通過在特定時間點測定接收室中的藥物濃度,評估受試藥物透皮吸收的行為。IVPT的供給側藥物,通常會使用藥物的過飽和溶液或制劑形式。主要原因是由于很多藥物的透皮行為是被動擴散機理,由兩側濃度差驅動,若供給側藥物濃度降低則透皮會變慢,因此在早期評估藥物透皮動力學參數時可能會使用過飽和溶液。但是當藥學研究進入處方篩選、等效性評估等階段時,則只需比較各輔料、處方組成之間的透皮差異即可。
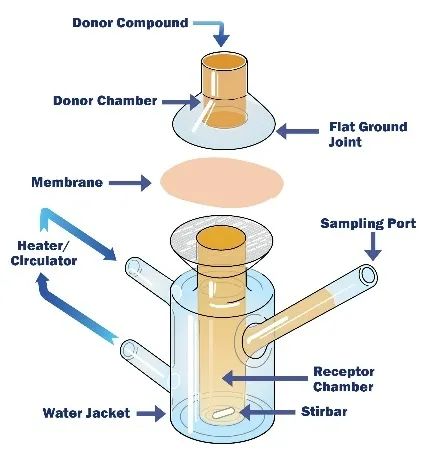
【圖1】典型的Franz擴散池的結構示意圖
通常,實驗中可能使用的皮膚包括人離體皮膚、豬耳部皮膚/乳豬皮膚、脫毛大鼠皮膚或裸鼠皮膚等。一般認為,各動物皮膚與人體皮膚滲透性的近似程度為豬耳部皮膚>脫毛大鼠皮膚>裸鼠皮膚,這可能與皮膚的厚度和毛囊數量有關。無論哪一個種屬的皮膚,都具有多層結構,其中最外側致密而疏水的角質層為皮膚提供了主要的屏障作用,可以有效抵御化學品或病原體等外來物質的侵入,但也是藥物經皮滲透最大的障礙。因此,若要客觀評估藥物的透皮行為,必須使用完整(主要是角質層無破損)的皮膚進行。目前各法規中對于此類實驗中皮膚的完整性評價都做了必要性的規定,FDA明確提出,僅使用目視觀察皮膚來評估完整性是不足夠的,可接受的皮膚完整性評價包括:氚水滲透、經表皮水損失、皮膚電阻/電導等。
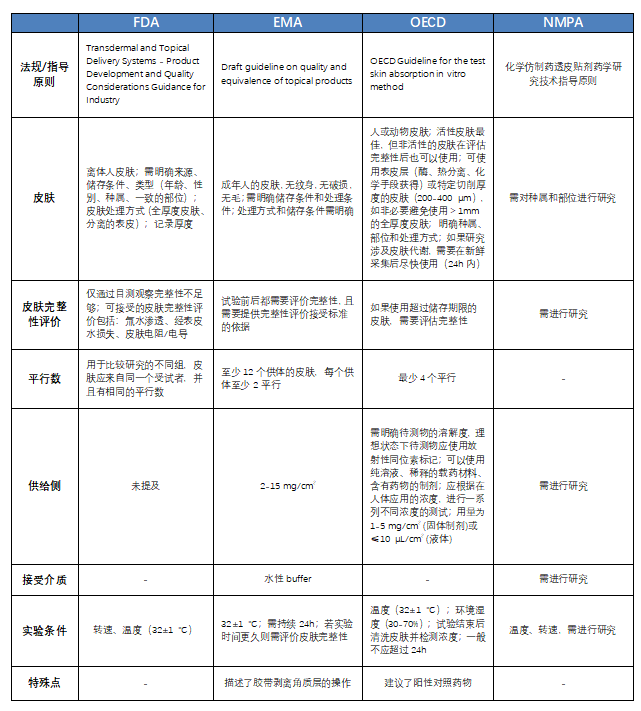
【表1】各主要藥監機構對于IVPT研究的法規/指導原則比較
一些IVPT在設計時除了要求在特定時間點測定接收室中的藥物濃度,還要在實驗結束時將皮膚取下,檢測皮膚中的藥物濃度,用以評估藥物的總回收率,以及皮膚局部用藥的駐留情況。一般來說只需要將皮膚勻漿,測定皮膚中總的藥物含量即可,但有些受試藥物出于特殊的考量,希望更為細致地測定皮膚各層結構中的藥物含量。EMA描述的膠帶剝離角質層法,就是用于此類研究目的的公認方式。使用普通膠帶按壓在皮膚上再快速撕去,重復約20次后,即可完全剝離皮膚上的角質層,且不損傷其下的活性表皮。然而這種方式面臨著從高分子膠粘劑中提取藥物的困難,同時,也不適用于貼劑的研究。
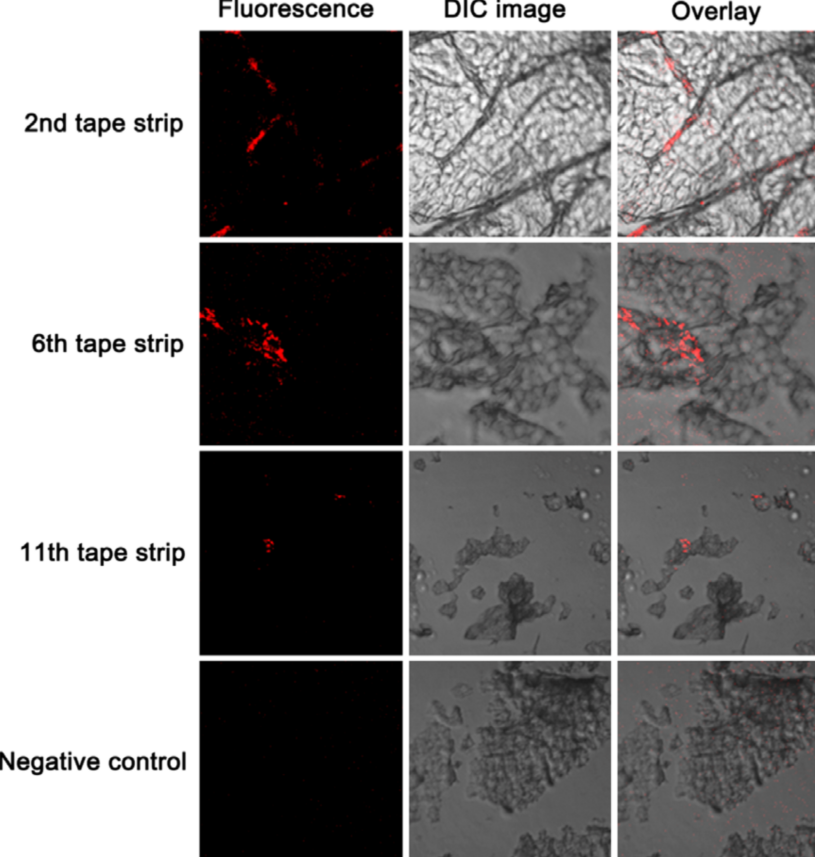
【圖2】在皮膚應用藥物后使用膠帶剝離角質層的共聚焦顯微鏡圖片
近些年較多的做法是直接使用組織切片機對實驗皮膚進行橫切,再分層測定濃度。然而,這種操作僅通過設定切片的厚度來實現,但實際上皮膚各層組織的厚度可能存在個體差異,且各層之間的結合是交錯的,并不是規整的平面,因此實際獲得的皮膚切片可能并不完全是所期待獲得的表皮層、真皮層等皮膚的生理結構分層,據此方法獲得的數據可能存在一定局限。
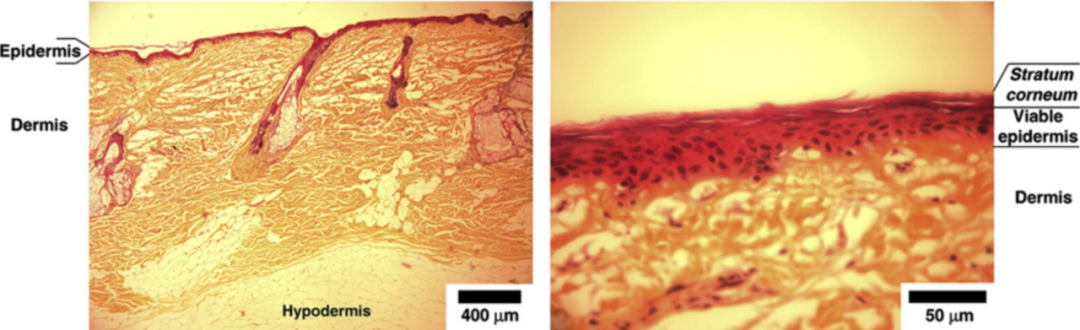
【圖3】光學顯微鏡下皮膚組織學特征,表皮層與真皮層之間的界面并不平整
與常見的口服、注射等制劑相比,皮膚外用制劑在給藥途徑上具有獨特的關注點和考察方式,因此在非臨床階段的評價需要格外注意。
參考文獻:
[1] S. H. Jeong, J. H. Kim, S. M. Yi, et al. Assessment of penetration of quantum dots through in vitro and in vivo human skin using the human skin equivalent model and the tape stripping method [J]. Biochemical and Biophysical Research Communications, 2010, 394
[2] M.-A. Bolzinger, S. Brian?on, J. Pelletier, et al. Penetration of drugs through skin, a complex rate-controlling membrane [J]. Current Opinion in Colloid & Interface Science, 2012, 17
[3] NMPA, 化學仿制藥透皮貼劑藥學研究技術指導原則(試行), 2020
[4] EMA, Draft guideline on quality and equivalence of topical products, 2019
[5] OECD, OECD Guideline for The Testing of Chemicals Skin Absorption: in vitro Method, 2004
[6] FDA, Transdermal and Topical Delivery Systems - Product Development and Quality Considerations Guidance for Industry, 2019
[7] 世界中醫藥學會聯合會經皮給藥專業委員會, 經皮給藥制劑體外經皮滲透試驗技術規范專家共識探討, 中國現代應用藥學[J], 2022, 39