藥物相互作用(Drug-Drug Interaction,DDI)研究貫穿新藥研發(fā)的整個周期,是指導(dǎo)臨床聯(lián)合用藥、優(yōu)化藥效方案以及指導(dǎo)個體化治療的重要依據(jù)。
藥物相互作用從機制上可劃分為:
① 藥代動力學(xué)相互作用:影響藥物在體內(nèi)的吸收、分布、代謝、排泄;
② 藥效動力學(xué)相互作用:影響藥物與受體的相互作用,改變其藥理效應(yīng)。
本文將從藥物的性質(zhì)、研究階段,不同指導(dǎo)原則要求等方面介紹轉(zhuǎn)運體介導(dǎo)的藥代動力學(xué)相互作用研究策略,對于代謝酶介導(dǎo)的DDI研究策略可參考我們之前發(fā)布的文章(ICH M12新規(guī)深度解讀:代謝酶介導(dǎo)的DDI研究策略全面升級)。
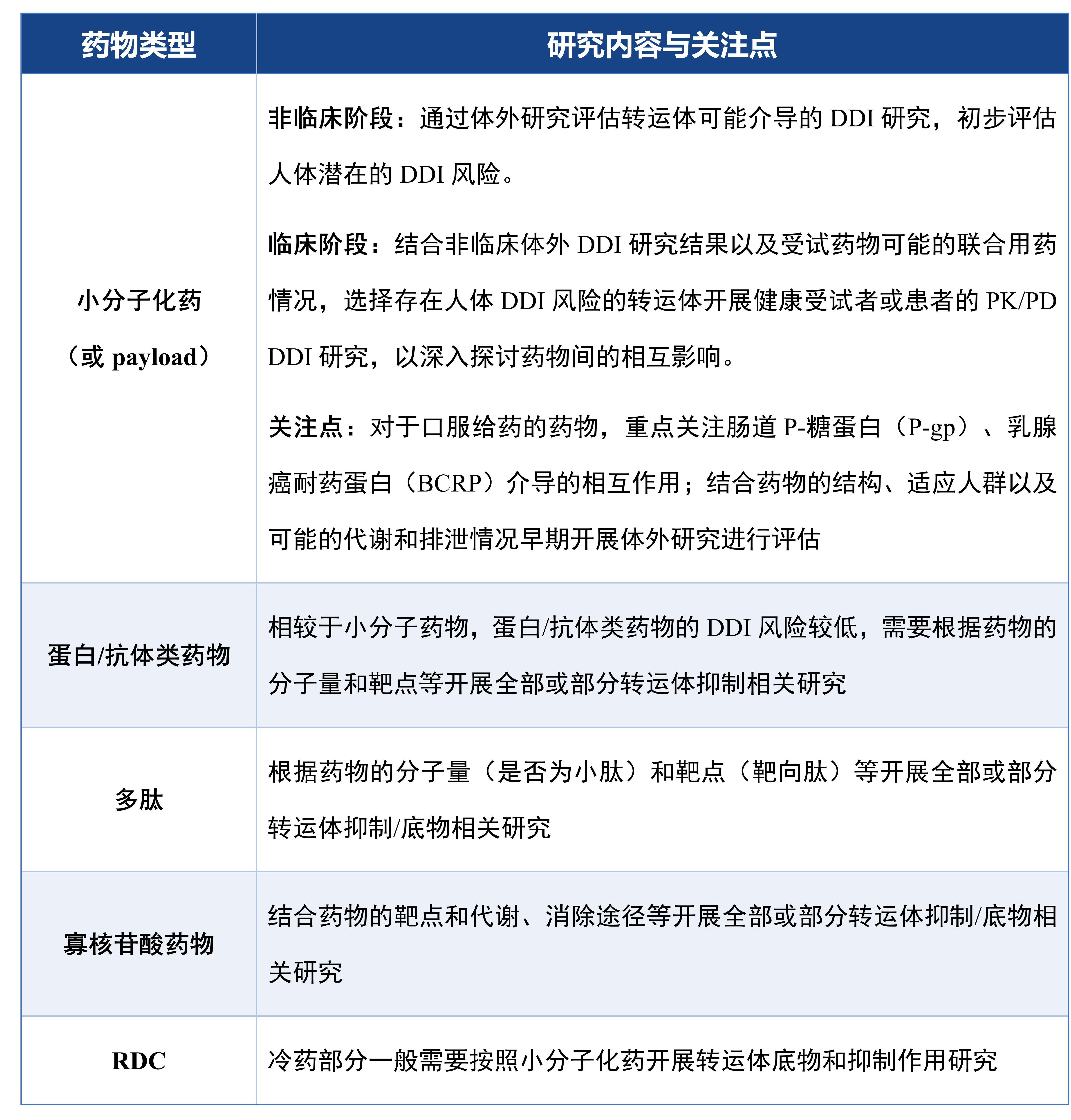
下表總結(jié)了不同類型藥物在不同的研發(fā)階段對于轉(zhuǎn)運體介導(dǎo)的DDI研究的內(nèi)容及要點。
一、轉(zhuǎn)運體介導(dǎo)的DDI研究指導(dǎo)原則
基于轉(zhuǎn)運體介導(dǎo)的藥物相互作用研究,歐洲藥品管理局(EMA)、美國食品藥品監(jiān)督管理局(FDA)、中國國家藥品監(jiān)督管理局(NMPA)分別在2013年、2020年、2021年頒布了相應(yīng)的藥物相互作用指導(dǎo)原則。為了減少企業(yè)在滿足多個監(jiān)管機構(gòu)要求時面臨的不確定性,國際人用藥品注冊技術(shù)協(xié)調(diào)會(ICH)在2024頒布了藥物相互作用研究的指導(dǎo)原則(ICH M12),該指導(dǎo)原則同樣也建議在研藥物開展轉(zhuǎn)運體介導(dǎo)的相互作用研究。
本文將進一步探討和比較ICH M12中對于體外轉(zhuǎn)運體介導(dǎo)的藥物相互作用評價的變更點并進行總結(jié)分析,進一步明確體外轉(zhuǎn)運體介導(dǎo)的DDI研究的評價標(biāo)準(zhǔn)。
二、轉(zhuǎn)運體的類型和主要表達(dá)部位
轉(zhuǎn)運體在體內(nèi)不同部位廣泛分布,是介導(dǎo)藥物吸收、分布、代謝、排泄的關(guān)鍵因素,主要分為:
① ABC轉(zhuǎn)運體家族(ATP結(jié)合盒轉(zhuǎn)運體):包括P-糖蛋白(P-gp)、乳腺癌耐藥蛋白(BCRP)、多藥耐藥相關(guān)蛋白(MRP)、膽汁鹽輸出泵(BSEP)等;
② SLC轉(zhuǎn)運體家族(溶質(zhì)載體轉(zhuǎn)運體):包括有機陰離子轉(zhuǎn)運多肽(OATP1B1/1B3/2B1)、有機陰離子轉(zhuǎn)運體(OAT1/3)、有機陽離子轉(zhuǎn)運體(OCT1/2)以及多藥及毒性化合物外排轉(zhuǎn)運蛋白(MATE1/2-K)等。
如下圖總結(jié)了不同轉(zhuǎn)運體的類型和主要表達(dá)部位:

三、轉(zhuǎn)運體介導(dǎo)的藥物相互作用評價
對于轉(zhuǎn)運體介導(dǎo)的DDI研究,主要研究:
① 轉(zhuǎn)運體對在研藥物的轉(zhuǎn)運作用;
② 在研藥物對轉(zhuǎn)運體的抑制作用;
③ 目前評價對轉(zhuǎn)運體誘導(dǎo)的體外方法尚不完善,未要求開展藥物對于轉(zhuǎn)運體的誘導(dǎo)作用。
1
?
ABC轉(zhuǎn)運體介導(dǎo)的藥物相互作用評價
ABC轉(zhuǎn)運體在底物轉(zhuǎn)運的過程中需要依賴ATP水解提供能量,其ATP的結(jié)合位點通常位于細(xì)胞內(nèi),主要介導(dǎo)底物的外排。目前已鑒定出的ABC轉(zhuǎn)運體有40多種,其中多藥耐藥(Multidrug Resistance, MDR)轉(zhuǎn)運體由于其在藥物耐藥和生理功能中的廣泛作用,已成為研究最廣泛的ABC轉(zhuǎn)運體,主要包括:P-gp,BCRP,MRPs等,也是各指導(dǎo)原則中推薦在藥物研發(fā)階段主要關(guān)注的ABC轉(zhuǎn)運體。
P-gp和BCRP:
其他ABC轉(zhuǎn)運體(如BSEP、MRP2):根據(jù)藥物的作用部位、吸收和消除途徑等綜合考慮,根據(jù)具體的情況分析是否需要進行研究。其中MRP2和BSEP是研究比較廣泛的轉(zhuǎn)運體。
MRP2是主要分布在腸道及肝臟的外排轉(zhuǎn)運體,通常在肝細(xì)胞基底膜和腎近曲小管上皮細(xì)胞等極性細(xì)胞的頂膜上表達(dá)。它參與多種毒性復(fù)合物的轉(zhuǎn)運,調(diào)節(jié)酸性配基的分泌,保護機體免受毒性陰離子的傷害。MRP2還是膽汁流的重要推動力,能促進膽汁的分泌和增加膽汁酸鹽的脂溶性;MRP2的表達(dá)下調(diào)與炎癥細(xì)胞因子的過度釋放和肝臟損傷密切相關(guān)。
BSEP是主要分布在肝細(xì)胞膽管側(cè)膜的外排轉(zhuǎn)運體,是肝細(xì)胞分泌膽酸鹽進入膽汁的主要轉(zhuǎn)運體,其變異和功能抑制與許多膽汁淤積癥和藥致肝損傷有關(guān)。
(1)試驗系統(tǒng)
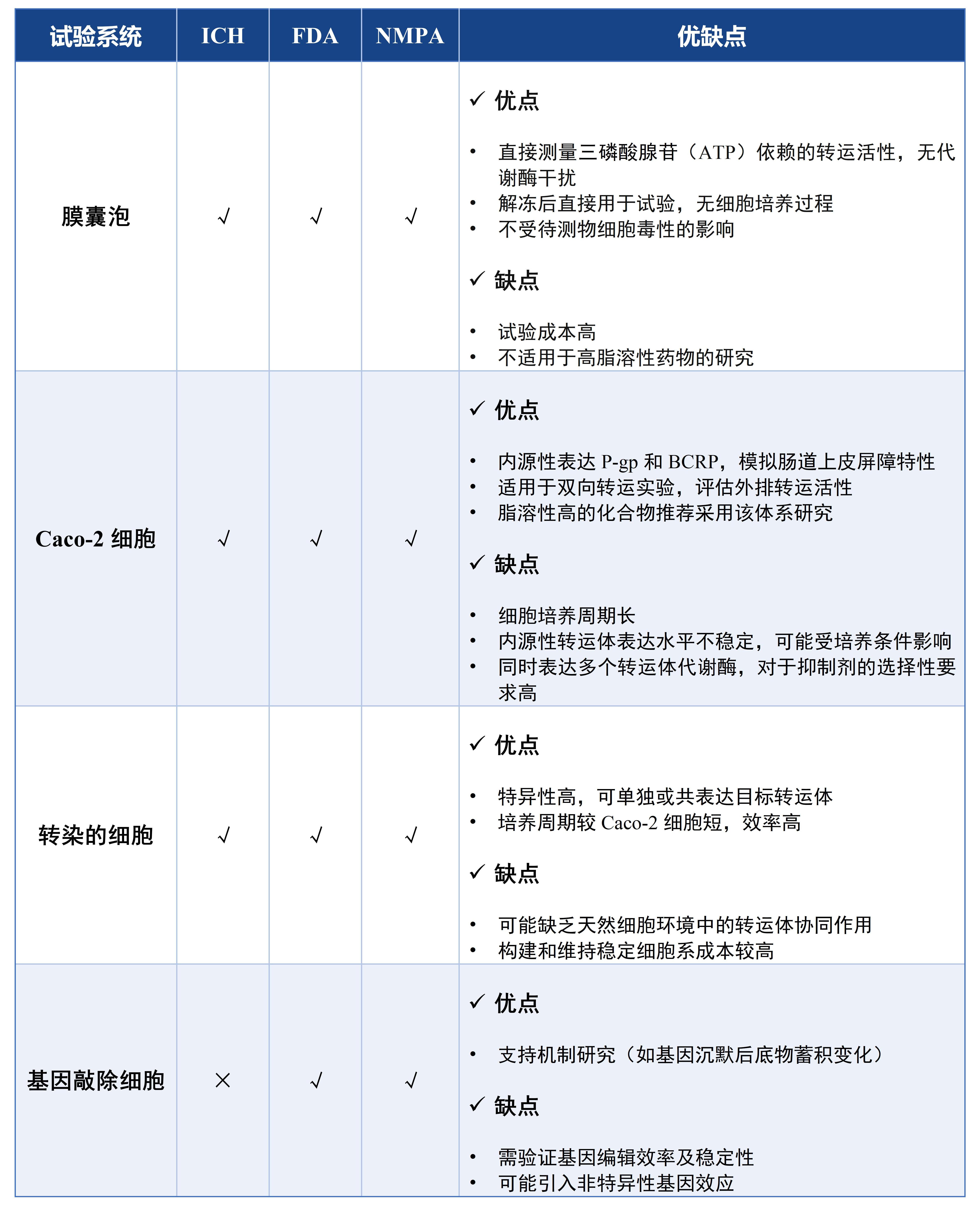
不同的監(jiān)管機構(gòu)對于開展ABC轉(zhuǎn)運體的研究均推薦了相應(yīng)的試驗系統(tǒng),下表總結(jié)和比較了ICH M12及其他監(jiān)管機構(gòu)(FDA、NMPA)對于開展體外ABC轉(zhuǎn)運體介導(dǎo)的DDI研究的試驗系統(tǒng)的異同點。
(2)ABC轉(zhuǎn)運體對在研藥物的轉(zhuǎn)運作用
下表總結(jié)和比較了不同監(jiān)管機構(gòu)對于ABC轉(zhuǎn)運體底物研究的方法及評價標(biāo)準(zhǔn)。ICH M12中刪除了對于特異性抑制劑濃度的限制,在實際執(zhí)行過程中需要在體系驗證和試驗過程中合理設(shè)置特異性抑制劑濃度。

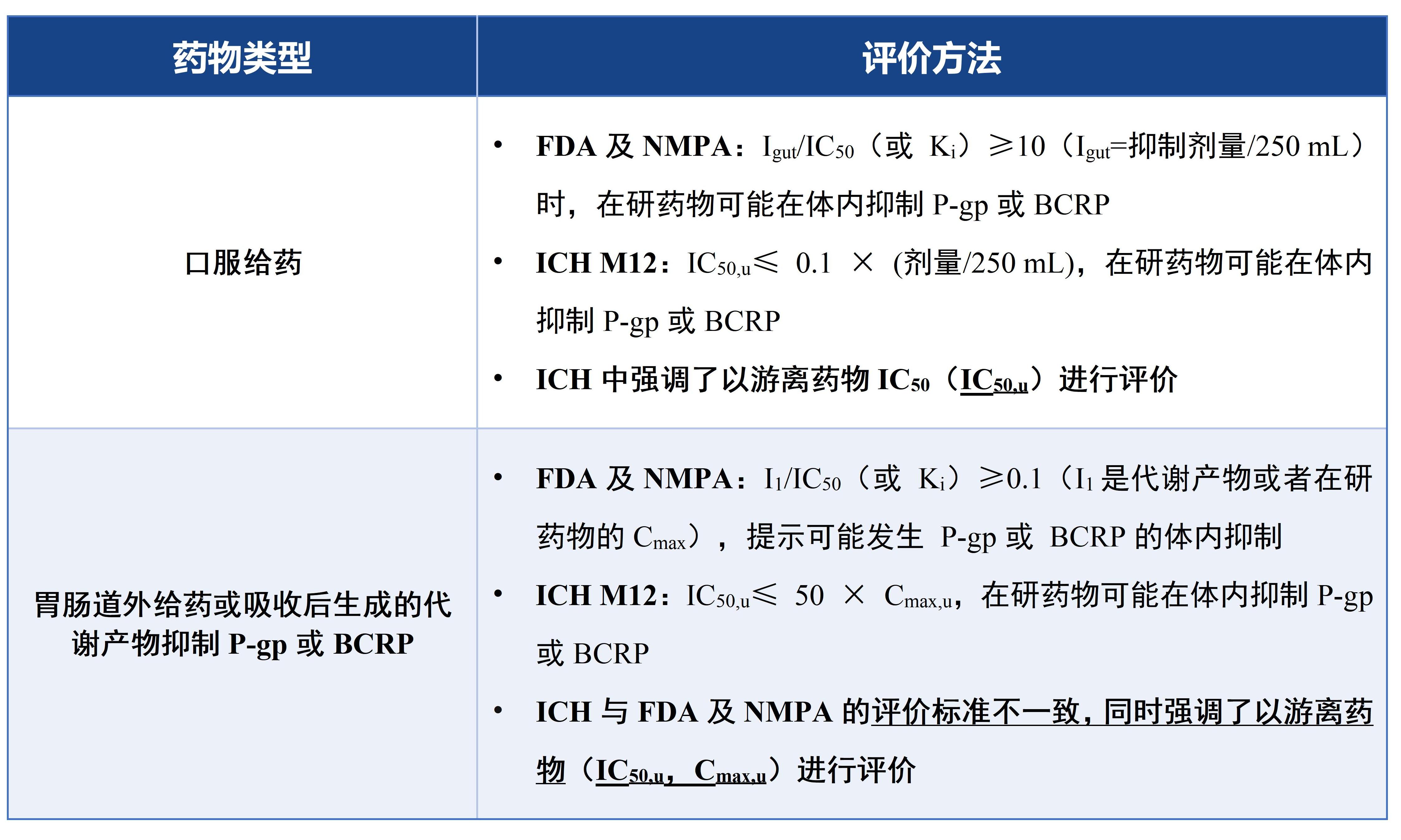
(3)在研藥物對ABC轉(zhuǎn)運體的抑制作用
在ICH M12指導(dǎo)原則中強調(diào)了以游離藥物進行評價,更符合實際的生理狀態(tài);另外,如果在研藥物的代謝產(chǎn)物是轉(zhuǎn)運體抑制劑或者在研藥物經(jīng)胃腸道外給藥,其對于P-gp及BCRP抑制作用評價的臨界值發(fā)生改變,較FDA及NMPA要求更嚴(yán)格。因此,建議以ICH M12中的臨界值作為推測臨床人體中藥物對ABC轉(zhuǎn)運體可能具有抑制作用的評估依據(jù)。
2
?
SLC轉(zhuǎn)運體介導(dǎo)的藥物相互作用評價
在藥物研發(fā)階段主要關(guān)注以下SLC轉(zhuǎn)運體:
OATP1B1和OATP1B3:
① 重要的肝臟攝取轉(zhuǎn)運體,主要分布在肝細(xì)胞的基底側(cè),影響藥物的肝臟代謝和膽汁排泄;
② 如藥物通過肝臟代謝或膽汁排泄在藥物的消除中占比≥25%,或者藥物的藥理學(xué)靶點在肝臟,則應(yīng)考察在研藥物是否為OATP1B1和1B3的底物。
OAT1/3、OCT2及MATE1/2-K:
①主要分布在腎臟,其中OAT1/3、OCT2主要分布在腎臟近端小管(基底外側(cè)膜),MATE1/2-K主要分布在腎臟近端小管(刷狀緣膜),參與藥物的腎臟主動分泌;
② 如果藥物的腎主動分泌清除率≥系統(tǒng)清除率的25%,則應(yīng)考慮對藥物進行體外研究,評價藥物是否為這些轉(zhuǎn)運體的底物。
其他SLC轉(zhuǎn)運:根據(jù)藥物的作用部位、吸收和消除途徑等綜合考慮,根據(jù)具體的情況分析是否需要進行研究。
(1)試驗系統(tǒng)
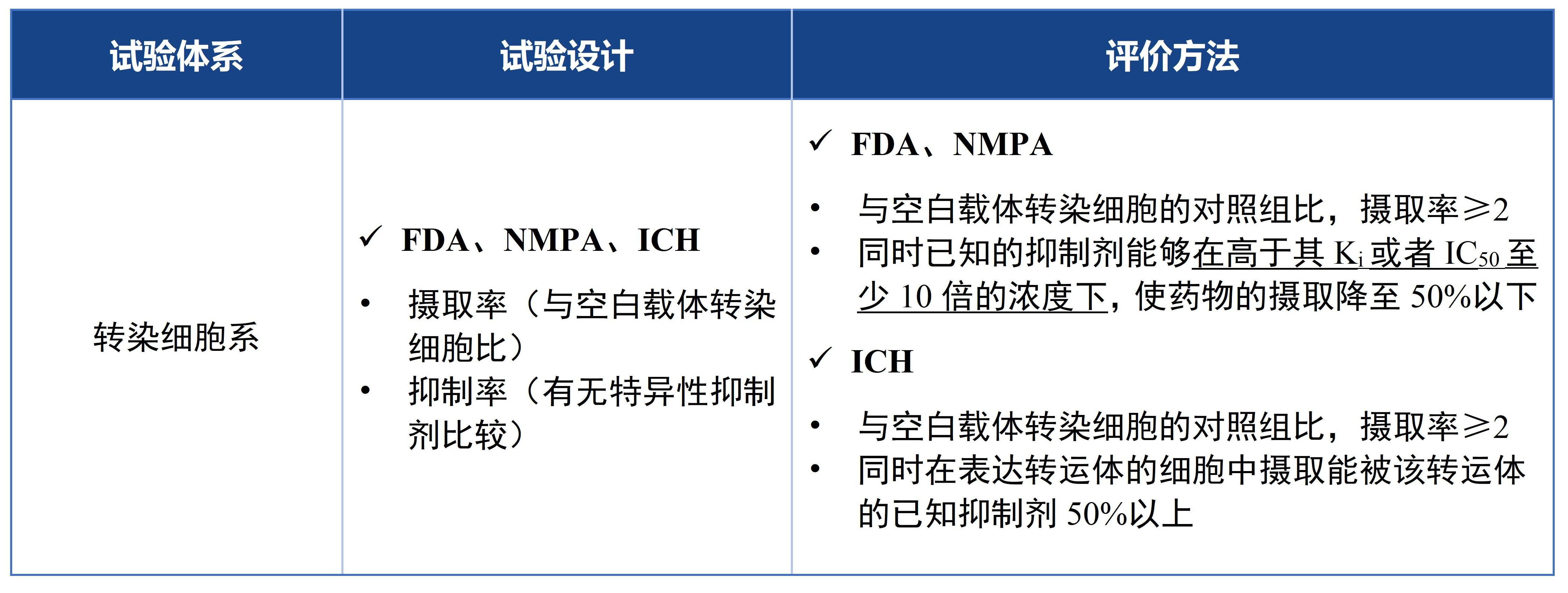
對于SLC轉(zhuǎn)運體介導(dǎo)DDI的體外評價體系,各監(jiān)管機構(gòu)的建議較為一致,一般建議采用轉(zhuǎn)染細(xì)胞系開展,除了轉(zhuǎn)染細(xì)胞系外也推薦采用懸浮或貼壁的人肝細(xì)胞進行研究。
(2)SLC轉(zhuǎn)運體對在研藥物的轉(zhuǎn)運作用
下表總結(jié)和比較了不同監(jiān)管機構(gòu)對于SLC轉(zhuǎn)運體底物研究的方法及評價標(biāo)準(zhǔn)。與ABC轉(zhuǎn)運體相同,在ICH M12中刪除了對于特異性抑制劑濃度的限制,在實際執(zhí)行過程中需要在體系驗證和試驗過程中合理設(shè)置特異性抑制劑濃度。
(3)在研藥物對SLC轉(zhuǎn)運體的抑制作用
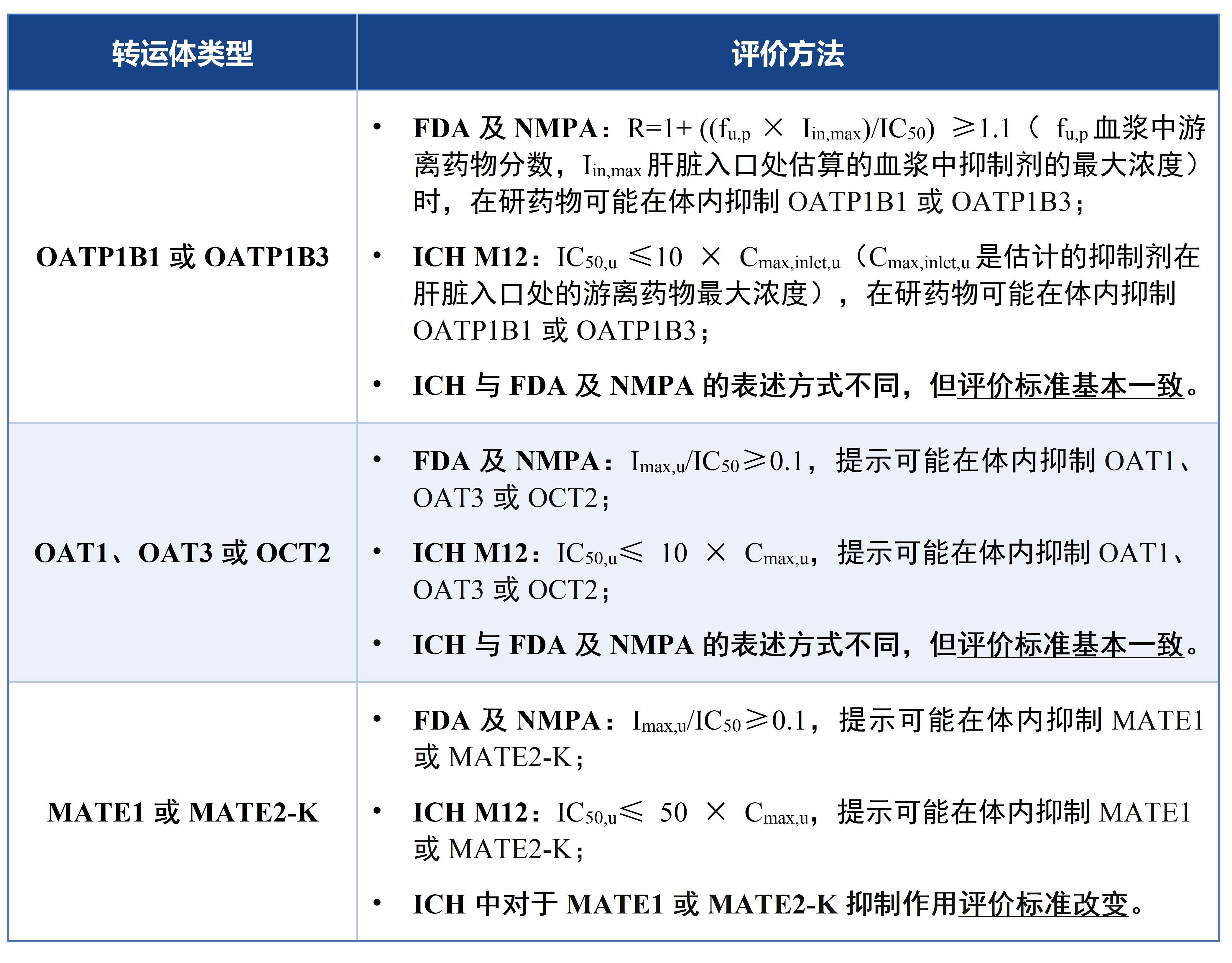
在體外研究中,通過測試不同濃度的在研藥物對SLC轉(zhuǎn)運體攝取/外排作用抑制的IC50值,評價在研藥物對轉(zhuǎn)運體的抑制作用。不同監(jiān)管機構(gòu)對于通過體外試驗數(shù)據(jù)評估在研藥物對人體轉(zhuǎn)運體的抑制作用的臨界值進行了規(guī)定,總結(jié)及比較見下表。在ICH M12指導(dǎo)原則中對于MATE1/MATE2-K抑制作用評價的臨界值發(fā)生改變,較FDA及NMPA要求更嚴(yán)格。
結(jié)語
隨著對轉(zhuǎn)運體研究的深入,指導(dǎo)原則中對于轉(zhuǎn)運體介導(dǎo)的DDI研究不斷的更新、細(xì)化,對新藥研發(fā)提出了新的要求與挑戰(zhàn)。有濟醫(yī)藥已完成多種體外轉(zhuǎn)運體研究模型的建立,積累了豐富的研究經(jīng)驗,具有完善的評估轉(zhuǎn)運體介導(dǎo)的DDI研究的DMPK技術(shù)平臺,同時根據(jù)指導(dǎo)原則的最新要求持續(xù)更新、完善,為新藥的研發(fā)提供更好的、全方位的技術(shù)服務(wù)。
參考文獻(xiàn):
[1]FDA Guidance for Industry: In Vitro Drug Interaction Studies —Cytochrome P450 Enzyme- and Transporter-Mediated Drug Interactions, January 2020.
[2]國家藥品監(jiān)督管理局(NMPA),藥物相互作用研究技術(shù)指導(dǎo)原則(試行),2021年1月
[3]International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human use —ICH Harmonised Guideline- Drug Interaction Studies M12, Endorsed on 21 May 2024.
[4]Aishwarya J, Srikanth P, Transporter-mediated drug–drug interactions: advancement in models, analytical tools, and regulatory perspective. Devi Swetha V. 2021 Aug;53(3).